Wikimedia Commons
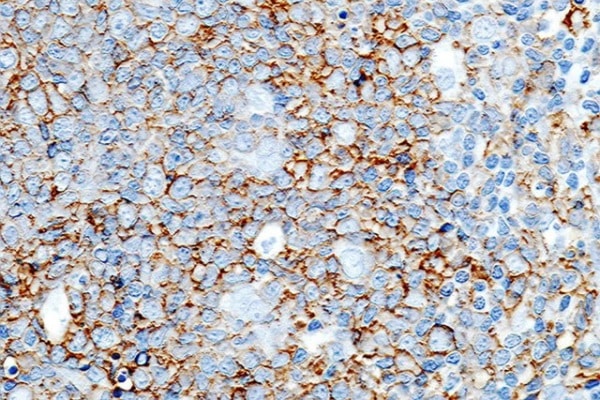
Linfoma difuso de grandes células B
Fonte
Rachel Tompa, Escola de Medicina da Universidade Stanford
Publicação Original
Áreas
Compartilhar
Resumo
Usando o conceito de apoptose celular, cientistas desenvolveram um novo método que une duas proteínas e religa um mecanismo de apoptose celular, que normalmente está desligado.
O método foi aplicado em linfoma difuso de grandes células B (LDGCB) em laboratório, e os resultados mostraram que a morte de células cancerígenas foi desencadeada com alta potência.
Foco do Estudo
Por que é importante?
Os tratamentos tradicionais para o câncer – quimioterapia e radioterapia – frequentemente eliminam um grande número de células saudáveis junto com as cancerosas.
Há anos, cientistas em todo o mundo estudam métodos para atacar precisamente as células cancerosas, evitando atingir células saudáveis.
Uma das estratégias é reverter algum mecanismo de proteção das células cancerosas de modo que fiquem fragilizadas a ataques do próprio sistema imune ou à imunoterapia, ou então que seja ativado algum mecanismo de destruição nas próprias células.
Estudo
Pesquisadores da Escola de Medicina de Stanford e do MD Anderson Cancer Center, nos EUA, usaram o conceito de apoptose (morte celular programada) para desenvolver uma nova abordagem terapêutica contra o câncer.
Para isso, foi criado um método que reúne artificialmente duas proteínas de tal forma que o novo composto ativa um conjunto de genes que podem estar envolvidos na morte de células cancerosas.
Uma dessas proteínas, a BCL6, quando mutada, impulsiona o câncer de sangue conhecido como linfoma difuso de grandes células B, e portanto é um oncogene. No linfoma, a BCL6 mutada fica no DNA perto dos genes promotores da apoptose e os mantém desligados, ajudando as células cancerosas a evitar a morte celular programada.
No novo estudo, os pesquisadores desenvolveram uma molécula que liga a BCL6 a uma proteína conhecida como CDK9, que atua como uma enzima que catalisa a ativação do gene, neste caso, ligando o conjunto de genes da apoptose que a BCL6 normalmente mantém desligado.
Essa abordagem — ligar algo que está desligado nas células cancerosas — contrasta com muitos outros tipos de terapias direcionadas ao câncer que inibem fatores específicos do câncer, desligando algo que normalmente está ligado.
O estudo foi publicado recentemente na revista científica Science.
Desde que os oncogenes foram descobertos, as pessoas têm tentado desligá-los no câncer. Em vez disso, estamos tentando usá-los para ligar a sinalização que, esperamos, será benéfica para o tratamento
Resultados
Quando a equipe testou a molécula em células de linfoma difuso de grandes células B no laboratório, eles descobriram que ela realmente matou as células cancerígenas com alta potência.
Eles também testaram a molécula em camundongos saudáveis e não encontraram efeitos colaterais tóxicos óbvios, embora a molécula tenha matado uma categoria específica de células B saudáveis dos animais, um tipo de célula imune, que também depende da BCL6. Eles agora estão testando o composto em camundongos com linfoma B difuso de grandes células para avaliar sua capacidade de matar o câncer em um animal vivo.
Como a técnica depende do suprimento natural das células de proteínas BCL6 e CDK9, ela parece ser muito específica para as células do linfoma — a proteína BCL6 é encontrada apenas neste tipo de célula de linfoma e em um tipo específico de célula B. Os pesquisadores testaram a molécula em 859 tipos diferentes de células cancerígenas no laboratório; o composto eliminou apenas células do linfoma difuso de grandes células B.
Mas como a BCL6 normalmente atua em 13 genes diferentes promotores de apoptose, os pesquisadores esperam que sua estratégia evite a resistência ao tratamento que parece tão comum no câncer. O câncer geralmente consegue se adaptar rapidamente a terapias que visam apenas um dos pontos fracos da doença, e algumas dessas terapias podem impedir o crescimento do câncer sem eliminar as células cancerosas completamente. A equipe de pesquisa espera que, ao impactar as células com vários sinais diferentes de morte celular de uma vez, o câncer não consiga sobreviver o suficiente para desenvolver resistência, embora essa ideia ainda precise ser testada.
O Dr. Gerald Crabtree, professor de Biologia do Desenvolvimento de Stanford, e o Dr. Nathanael Gray, pesquisador de Bioquímica e Biologia de Sistemas de Stanford e coautor sênior do estudo, são cofundadores de uma startup de biotecnologia, a Shenandoah Therapeutics, que visa testar ainda mais essa molécula e uma molécula semelhante, desenvolvida anteriormente, na esperança de reunir dados pré-clínicos suficientes para dar suporte ao lançamento de ensaios clínicos dos compostos.
Eles também planejam construir moléculas semelhantes que poderiam ter como alvo outras proteínas causadoras de câncer, incluindo o oncogene Ras, que é um fator causador de vários tipos diferentes de câncer.
A ideia é: considerar algo de que o câncer depende para sua sobrevivência e inverter o roteiro, fazer com que isso seja exatamente o que o mata
Em suas publicações, o Portal SciAdvances tem o único objetivo de divulgação científica, tecnológica ou de informações comerciais para disseminar conhecimento. Nenhuma publicação do Portal SciAdvances tem o objetivo de aconselhamento, diagnóstico, tratamento médico ou de substituição de qualquer profissional da área da saúde. Consulte sempre um profissional de saúde qualificado para a devida orientação, medicação ou tratamento, que seja compatível com suas necessidades específicas.
Autores/Pesquisadores Citados
Instituições Citadas
Publicação
Acesse o resumo do artigo científico (em inglês).
Acesse a revista científica Science (em inglês).
Mais Informações
Acesse a notícia original completa na página da Escola de Medicina da Universidade Stanford (em inglês).
Notícias relacionadas
Outros avanços

Universidade Politécnica de Madri
Universidade de Sydney
Universidade de Sevilha